Интерполяция свойств химических элементов
Идея интерполяции свойств элементов возникла в химии еще до создания периодической системы [7.7]. В триадах Деберейнера (1817г.) характеристики среднего элемента триады находились как средние арифметические значений характеристик крайних элементов. Были попытки работать с тетрадами, "эннеадами" (составленными из трех триад) и т.п. Периодическая таблица Менделеева позволяет по-разному определять группу ближайших соседей для интерполяции: от двух вертикальных соседей по ряду таблицы до окружения из восьми элементов (два из того же ряда и по три из соседних рядов). Однако интерполяция свойств путем взятия среднего арифметического по ближайшим элементам таблицы не всегда (не для всех свойств и элементов) дает приемлемые результаты - требуется либо иной выбор соседей, либо другая процедура интерполяции.
Более общим образом задачу интерполяции можно поставить так: найти для каждого элемента наилучшую формулу, выражающую его вектор свойств через векторы свойств других элементов. Эту задачу и решает метод транспонированной регрессии.
В работах [7.9, 7.10] исследовался полуэмпирический метод, близкий по идее к методу транспонированной регрессии. Единственное и главное отличие заключалось в том, что среди параметров сразу фиксировался набор "теоретических" и строились зависимости остальных свойств от них (в частности, зависимости потенциалов ионизации от атомного номера).
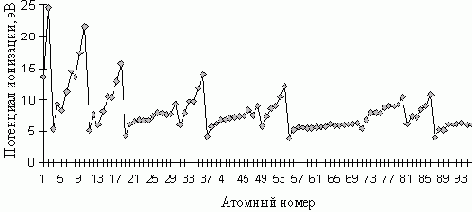
Рис. 7.1. Зависимость 1-го ПИ от атомного номера
Используем метод транспонированной линейной регрессии для интерполяции и прогноза высших потенциалов ионизации (ПИ). Напомним, что n-й потенциал ионизации A - энергия, которую необходимо затратить, чтобы оторвать n-й электрон от иона A(n-1)+ (n-1 раз ионизированного атома A). Зависимость ПИ от атомного номера ( рис. 7.1) нелинейна и сложна.
Следуя формальному смыслу, n-й ПИ атома A следует относить все к тому же атому. Однако структура энергетических уровней иона определяется зарядом ядра и числом электронов. Для атома оба этих числа совпадают с атомным номером, но для ионов уже различны.
Удовлетворительная точность достигается при трех и четырех элементах в опорной группе.
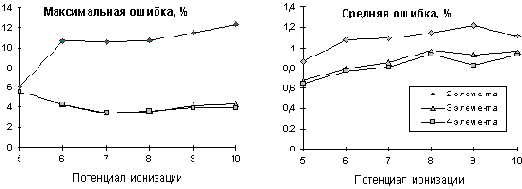
Рис. 7.3. Зависимость ошибок прогноза 5-10 ПИ от числа элементов в опорной группе. Опорные группы и регрессионные зависимости строились по первым четырем ПИ
Дальнейшее увеличение числа элементов в опорной группе себя не оправдывает. Увеличению точности прогноза мешают и погрешности при экспериментальном определении ПИ, особенно высших. В таблице 7.2 таблица 7.2 приводится прогноз отсутствующих значений ПИ.
| 59 | Pr | 50,7 | |||||
| 60 | Nd | 49,2 | 69,6 | ||||
| 61 | Pm | 53,6 | 67,7 | 97,1 | |||
| 62 | Sm | 55,9 | 72,9 | 87,9 | 123,7 | ||
| 63 | Eu | 56,3 | 76,3 | 93,9 | 110,8 | 153,6 | |
| 64 | Gd | 61,9 | 77,2 | 98,4 | 117,7 | 135,9 | 186,9 |
| 65 | Tb | 67,4 | 84,9 | 99,8 | 123,8 | 142,9 | 63,8 |
| 66 | Dy | 48,3 | 92,2 | 110,2 | 125,9 | 151,5 | 171,3 |
| 67 | Ho | 52,6 | 65,8 | 119,5 | 138,0 | 154,5 | 181,6 |
| 68 | Er | 54,5 | 72,1 | 84,6 | 149,7 | 169,1 | 185,7 |
| 69 | Tm | 54,9 | 74,5 | 93,4 | 106,1 | 182,8 | 203,5 |
| 70 | Yb | 52,4 | 74,8 | 96,1 | 117,3 | 128,6 | 219,9 |
| 71 | Lu | 57,8 | 71,7 | 96,2 | 120,6 | 143,9 | 154,0 |
| 72 | Hf | 63,1 | 79,2 | 92,2 | 121,0 | 147,8 | 173,2 |
| 73 | Ta | 85,8 | 102,4 | 115,2 | 147,4 | 177,1 | |
| 74 | W | 110,5 | 128,2 | 140,7 | 176,6 | ||
| 75 | Re | 139,0 | 156,9 | 168,7 | |||
| 76 | Os | 170,1 | 188,6 | ||||
| 77 | Ir | 203,7 |
Как и в работах [7.9, 7.10], n-й потенциал ионизации атома с атомным номером m будем искать как функцию от m-n+1. Объектами будут служить, строго говоря, не атомы с атомным номером m, а m-электронные системы. Таким образом, второй ПИ гелия (атомный номер 2), третий ПИ лития (атомный номер 3) и т.д. относятся к одноэлектронной системе при различных зарядах ядра. Осуществляется привязка потенциала ионизации уже ионизированного атома не к этому же атому, а к m-электронной системе с m, равным имеющемуся числу электронов в ионе.
Рассмотрим результаты пробного прогноза высших потенциалов ионизации. Приведем результаты, полученные при использовании в функции критерия нормы в виде суммы абсолютных значений компонент вектора и значения

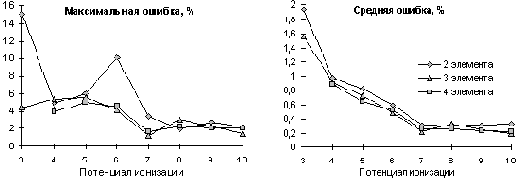
Рис. 7.2. Зависимость ошибки прогноза 3-10 ПИ от числа элементов в опорной группе. Опорные группы и регрессионные зависимости для каждого ПИ строились по предыдущим ПИ
На рис. 7.2 показаны ошибки прогноза ПИ (с 3-го по 10-й) при разных размерах опорных групп (2, 3 и 4 элемента в опорной группе). При этом для каждого ПИ опорные группы строились по предыдущим ПИ. Величины максимальной и средней ошибок показаны в процентах от диапазона изменения величин соответствующего ПИ. На основе приведенных графиков можно рекомендовать использование как можно большего набора однородных свойств для достижения оптимального прогноза.
Для попытки прогноза отсутствующих в справочной литературе [7.11, 7.12] значений высших ПИ (с 5-го по 10-й ПИ для элементов с атомными номерами от 59-го до 77-го) изучим влияние размера опорной группы на точность прогноза при построении опорной группы по первым четырем ПИ ( Рис. 7.3).
Удовлетворительная точность достигается при трех и четырех элементах в опорной группе.
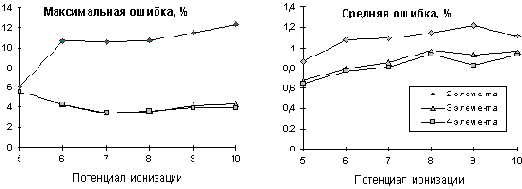
Рис. 7.3. Зависимость ошибок прогноза 5-10 ПИ от числа элементов в опорной группе. Опорные группы и регрессионные зависимости строились по первым четырем ПИ
Дальнейшее увеличение числа элементов в опорной группе себя не оправдывает. Увеличению точности прогноза мешают и погрешности при экспериментальном определении ПИ, особенно высших. В таблице 7.2 таблица 7.2 приводится прогноз отсутствующих значений ПИ.
| 59 | Pr | 50,7 | |||||
| 60 | Nd | 49,2 | 69,6 | ||||
| 61 | Pm | 53,6 | 67,7 | 97,1 | |||
| 62 | Sm | 55,9 | 72,9 | 87,9 | 123,7 | ||
| 63 | Eu | 56,3 | 76,3 | 93,9 | 110,8 | 153,6 | |
| 64 | Gd | 61,9 | 77,2 | 98,4 | 117,7 | 135,9 | 186,9 |
| 65 | Tb | 67,4 | 84,9 | 99,8 | 123,8 | 142,9 | 63,8 |
| 66 | Dy | 48,3 | 92,2 | 110,2 | 125,9 | 151,5 | 171,3 |
| 67 | Ho | 52,6 | 65,8 | 119,5 | 138,0 | 154,5 | 181,6 |
| 68 | Er | 54,5 | 72,1 | 84,6 | 149,7 | 169,1 | 185,7 |
| 69 | Tm | 54,9 | 74,5 | 93,4 | 106,1 | 182,8 | 203,5 |
| 70 | Yb | 52,4 | 74,8 | 96,1 | 117,3 | 128,6 | 219,9 |
| 71 | Lu | 57,8 | 71,7 | 96,2 | 120,6 | 143,9 | 154,0 |
| 72 | Hf | 63,1 | 79,2 | 92,2 | 121,0 | 147,8 | 173,2 |
| 73 | Ta | 85,8 | 102,4 | 115,2 | 147,4 | 177,1 | |
| 74 | W | 110,5 | 128,2 | 140,7 | 176,6 | ||
| 75 | Re | 139,0 | 156,9 | 168,7 | |||
| 76 | Os | 170,1 | 188,6 | ||||
| 77 | Ir | 203,7 |


 | © 2003-2007 INTUIT.ru. Все права защищены. |